EBMT2022 中国之声 | 2年总生存率79%,2年无病生存率79%!Allo-HSCT显著改善R/R Ph+ ALL预后
2022年3月19日~23日,第48届欧洲血液与骨髓移植年会(2022 EBMT)于布拉格隆重召开。在这个久负盛名的国际造血干细胞移植领域的盛会上,众多中国学者带来精彩纷呈的学术成果,闪耀中国智慧,贡献中国力量。
其中,高博医学血液病(北京研究中心)北京博仁医院吴彤主任团队宋艳智主任分析了异基因造血干细胞移植(allo-HSCT)在复发/难治(R/R)的费城染色体阳性(Ph+)急性B淋巴细胞白血病(B-ALL)中的疗效与安全性,研究成果以壁报形式精彩亮相2022 EBMT盛会。为此,我们特别邀请吴彤主任解读研究内容,阐明临床意义,把脉发展方向。
病例与方法
研究纳入了2018年11月至2021年11月期间在北京博仁医院接受allo-HSCT治疗的29例R/R Ph+ B-ALL患者。中位年龄为28(3-59)岁,中位病程为21(5-59)个月。移植前所有患者均达到完全缓解(CR),其中21/29例(72.4%)通过嵌合抗原受体T细胞(CAR-T)治疗获得CR。
移植前8例(27.6%)为微小残留病(MRD)阳性(流式检测阳性2例,RT-PCR检测融合基因阳性6例),11例(37.9%)伴有T315I突变,有5例(17.2%)为二次allo-HSCT。
移植类型:2例为同胞相合移植,19例为亲缘半相合移植,8例为非血缘移植(供受者HLA 10/10或 9/10相合)。
清髓预处理方案:分次全身照射/依托泊苷/氟达拉滨或环磷酰胺/兔抗人胸腺细胞球蛋白(ATG)。
移植物抗宿主病(GVHD)的预防:环孢素、霉酚酸酯和短程甲氨蝶呤。
维持治疗:所有患者在移植后均接受了敏感的酪氨酸激酶抑制剂(TKI)的维持治疗至移植后2年。
结果
所有患者均获得了持久造血重建。中位随访时间为8(1-36)个月,2年总生存率(OS)为79%,2年无病生存率(LFS)为 79%。随访期间只有2例患者复发,其中1例患者死于复发,另1例正在接受移植后的供者CAR-T治疗。
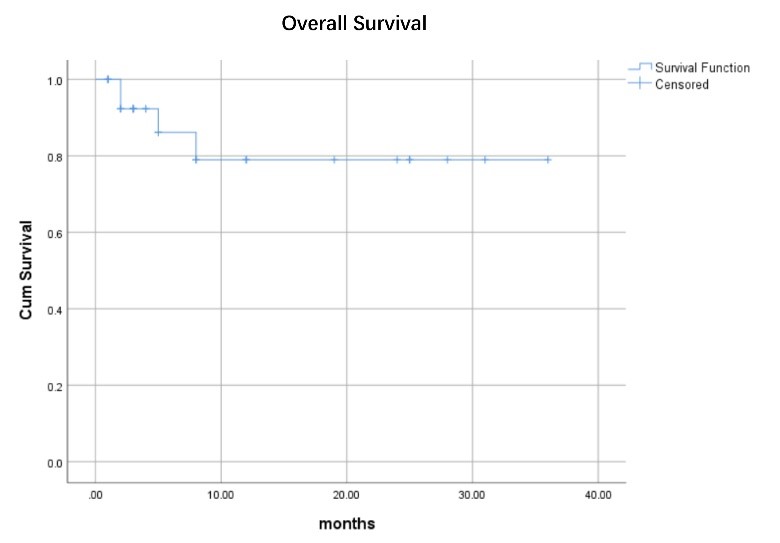
图1:患者2年总OS数据结果
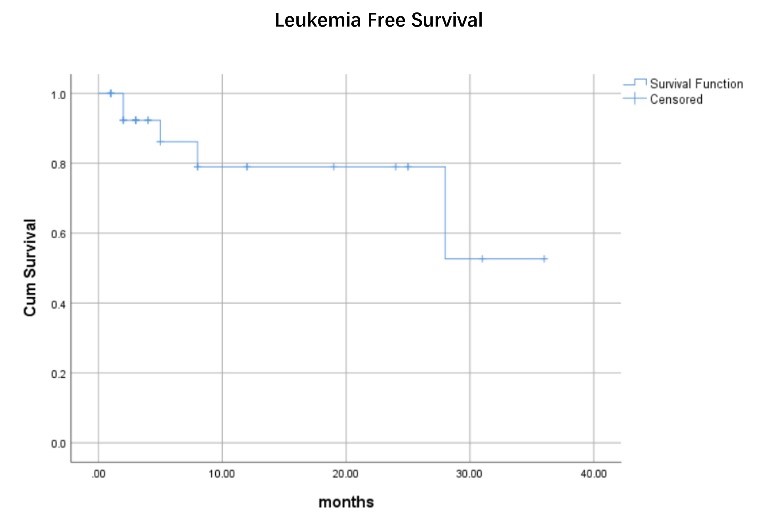
图2:患者2年总LFS数据结果
3例患者出现了Ⅲ~Ⅳ度急性GVHD(aGVHD),2例患者发生广泛型慢性GVHD(cGVHD),2例患者死于Ⅳ度aGVHD,其余患者治疗后GVHD缓解。
此外,1例患者在移植后7个月死于严重病毒性肺炎;7例患者出现巨细胞病毒(CMV)再激活,没有患者出现EB病毒(EBV)再激活;5例患者出现轻度出血性膀胱炎;1例患者发生严重细菌性肺炎,经抗生素治疗后痊愈。
总体非复发死亡率(NRM)为10.3%(3/29)。针对11例伴有T315I突变患者的分析显示,2年的OS和LFS均为87.5%,仅有1例患者复发,并死于复发,没有患者死于移植相关的不良事件;针对21例经CAR-T治疗获得CR患者的分析显示,2年的OS和LFS均为85.3%,NRM为9.5%;针对8例移植前MRD阳性患者的分析显示,仅1例患者在移植后28个月复发,没有出现移植相关的死亡。
结论
我们的研究表明,采用上述治疗方案,对于R/R Ph+ B-ALL患者而言,allo-HSCT是一种非常有效且安全的治疗方法,2年OS和LFS均可达到79%,并且移植相关死亡率低(3/29)。即使对于移植前伴有T315I突变或MRD阳性的患者,allo-HSCT亦能带来显著的生存获益。
吴彤主任解读
Ph+ ALL为高危疾病,自TKI靶向药物问世以来,显著提高了此类疾病的诱导缓解率,特别是缓解深度,从而使部分患者可以通过TKI联合化疗达到持续的MRD阴性的CR甚至治愈,显著改善了此类患者的预后。
但仍有部分患者原发难治,或治疗过程中复发,或产生T315I等耐药突变,或TKI副作用不能耐受等,这时可选择的治疗包括CAR-T、CD3/CD19双抗、三代TKI类药物、化疗、allo-HSCT等。
我们团队和许多其它团队的研究结果均显示CD19-CAR-T可使80%-90%的R/R B-ALL达到CR1,2,但成人的临床试验结果显示CD19-CAR-T后1年的累计复发率为67.9%3,而R/R ALL挽救性allo-HSCT的OS仅约30%,因此我们采用CAR-T后桥接allo-HSCT的策略,使此类患者的LFS提高到73%4。
在本研究中,大部分患者(21/29例)为标准治疗(TKI联合化疗)无效或失败者,经CAR-T达到CR后桥接allo-HSCT,2年的LFS达到85.3%,并不比Ph- ALL的移植结果差。尤其值得关注的是,移植前出现T315I突变并没有对allo-HSCT的结果产生不良影响,这组患者2年的LFS高达87.5%。
Allo-HSCT并不是终极治疗,对于R/R Ph+ B-ALL患者而言,移植后采用敏感的TKI类靶向药物做维持治疗,可显著降低移植后的复发率。此外,采用含全身照射的预处理方案也是降低移植后复发率的有效手段5。
不断涌现的靶向药物、CAR-T免疫治疗等新的治疗手段,给患者带来更精准的治疗,取得更深度的完全缓解,这些治疗与allo-HSCT的恰当结合必将使更多的患者获得治愈。
参考文献
